Publicado en Alambique
Aureli Caamaño
IES Barcelona-Congrés
Josep Corominas
Escola Pia (Sitges)
Gran parte de la ineficacia de los trabajos prácticos se atribuye a su presentación con un formato cerrado, es decir, como un conjunto de instrucciones que los estudiantes deben seguir sin darles ocasión para que se den cuenta de cuál es el problema que se pretende resolver ni cómo puede ser resuelto. Frente a esta manera de presentar los trabajos prácticos, proponemos una forma abierta en la que se plantee el problema a resolver de una forma contextualizada y se ayude a los estudiantes a pensar de qué manera pueden resolverlo a través de una serie de cuestiones estructuradas, que constituyan la base de un diálogo entre profesor y estudiantes y entre estudiantes entre sí. La propuesta se ilustra mediante el planteamiento y resolución del problema de la determinación de la masa atómica relativa del magnesio.
Introducción
Diversos autores (Qualter et al. 1992, Watson 1994, Carrascosa 1995, Gott y Dugan 1995; Gil y Valdés 1996: Oldworthy y Watson 2001; Martins 2002; Caamaño 2002, 2003; Gárritz 2004,;Hernández 2004) han defendido el interés de la utilización de trabajos prácticos abiertos o investigaciones en las clases de ciencias. La investigación que se expone a continuación, ¿Cómo determinar la masa atómica relativa del magnesio?, plantea un problema que fue de gran interés en el establecimiento y consolidación de la teoría atomicomolecular de Dalton. Constituye, por tanto, un ejemplo del tipo de trabajo práctico que hemos clasificado como investigación para resolver un problema teórico (Caamaño 2003). Como actividad práctica en la escuela ha sido experimentada por nosotros durante varios años en clases de química de bachillerato y forma parte del dosier de trabajos prácticos de los cursos de formación del profesorado sobre este tema, que se han venido realizando en Cataluña en estos dos últimos años (Caamaño, Corominas 2002).
En la descripción de esta investigación intentaremos reproducir en la medida de lo posible la dinámica que se establece en el aula cuando este tipo de problemas se plantean, se planifican y se resuelven a través de las preguntas clave que se plantean a los estudiantes. La investigación transcurre a través de las siguientes fases: presentación y comprensión del problema a resolver, planificación del método a seguir y de los cálculos a realizar, realización del experimento o de las medidas, tratamiento de los datos, evaluación del resultado y comunicación de la investigación realizada. Nos centraremos especialmente en las dos primeras fases: la presentación y comprensión del problema, y la planificación. La descripción que hacemos de estas fases corresponde a un diálogo del profesor o profesora con el conjunto del grupo-clase, que puede mantenerse de forma inmediata a las cuestiones que se plantean o después de haber dejado pensar a los estudiantes, por parejas o en grupo, durante un corto periodo de tiempo.
Un ejemplo: ¿Cómo determinar la masa atómica relativa del magnesio?
PLANTEAMIENTO DEL PROBLEMA
El planteamiento de este problema requiere situarlo en el contexto histórico en que fue relevante, a inicios del siglo XIX, cuando Dalton formuló la teoría atómica de la materia y señaló la masa atómica como una de las propiedades diferenciadoras de cada elemento químico. Este problema es de interés en el marco escolar en la introducción y justificación de la teoría atómicomolecular que se realiza en el primer curso de química del bachillerato. Como es sabido, para la determinación de las masas atómicas relativas de los átomos, los químicos de la época de Dalton tomaron como referencia la masa del átomo de hidrógeno, por ser el elemento más ligero.
PLANIFICACIÓN DEL PROCEDIMIENTO EXPERIMENTAL Y DE CÁLCULO
Una primera aproximación a la resolución del problema planteado
Alguno de los estudiantes puede contestar: “Haciendo reaccionar el magnesio con otro de masa atómica relativa conocida, y midiendo las masas que reaccionan de cada elemento”. Es una buena solución. Claro que para poder deducir, a partir de las masas que han reaccionado, cúal es la relación entre las masas de los átomos, es preciso suponer el número de átomos que reaccionan de cada elemento. ¡Y esto es lo que no sabían con seguridad los químicos de la época de Dalton! Pero nosotros vamos a tenerlo más fácil, porque vamos a partir ya del conocimiento de la estequiometría de la reacción.
¿Qué reacción podemos utilizar?
La respuesta más probable, después de la introducción realizada, será proponer la reacción del magnesio con el hidrógeno. Pero, ésta no es una reacción fácil de llevar a la práctica. ¿No podríamos utilizar una reacción más fácil de realizar, aunque el hidrógeno no apareciera como reactivo sino como producto? ¿Qué reacción del magnesio produce hidrógeno? “La reacción del magnesio con un ácido”, puede contestar cualquier estudiante. En efecto, la típica reacción de un metal activo con un ácido. Si utilizáramos ácido clorhídrico, la ecuación de la reacción sería:
Mg(s) + 2HCl(aq) = MgCl2(aq) + H2(g)
¿Qué medidas y qué cálculos es preciso realizar?
Una posible respuesta: “Medir la masa del magnesio que reacciona y la masa del hidrógeno que se forma”. Con estas masas podríamos establecer la relación siguiente:
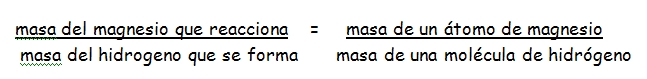
Y teniendo en cuenta que la masa de una molécula de hidrógeno es igual a dos veces la masa de un átomo de hidrógeno, podríamos determinar la relació:

que es justamente la masa atómica relativa del magnesio, Ar(Mg), de acuerdo con la definición con que trabajamos.
Llegados a este punto, ya tenemos el marco de referencia teórico y procedimental sobre el que basar la resolución del problema propuesto, ahora nos es preciso pensar cómo lo haremos en la práctica, es decir, el procedimiento experimental. Las preguntas que nos hacemos son ¿cómo medir la masa de magnesio? y ¿cómo medir la masa de hidrógeno?
¿Cómo medir la masa del magnesio y la masa del hidrógeno?
El profesor tiene aquí dos posibilidades para regular el grado de apertura de la investigación, mostrar el material de laboratorio que puede utilizarse o no hacerlo. Quizás una buena opción sea no hacerlo en primera instancia y reservarse la posibilidad de mostrarlo más adelante. En cualquier caso, la medida de la masa de magnesio no ofrece gran dificultad, ya que se puede hacer con unas balanzas antes de iniciar la reacción. Algo más complicado es la medida de la masa del hidrógeno que se desprende, por tratarse de un gas.
Un estudiante de CAP (curso de formación inicial) nos respondió recientemente lo siguiente en una sesión en que planteamos esta cuestión: “Podríamos pesar el sistema reaccionante (vaso, magnesio y solución de ácido clorhídrico) al inicio y al final y, por diferencia, obtener la masa del hidrógeno que se ha producido”. Éste es evidentemente el procedimiento más sencillo, lo que ocurre es que presenta algunos inconvenientes. Debido a la pequeña densidad del hidrógeno gas, sería necesario utilizar una relativa importante cantidad de magnesio para poder apreciar con las balanzas de que disponemos la disminución de la masa debido al hidrógeno que se escapa. Y hacer esto no es muy aconsejable teniendo en cuenta que el hidrógeno es muy inflamable. Pero, aún teniendo en cuenta este riesgo, la propuesta no es en absoluto desacertada y de la discusión de sus problemas potenciales podemos obtener siempre un provecho.
Si descartamos esta opción aparece otra posibilidad: recoger el hidrógeno que se desprende y medir su volumen, y realizar una determinación indirecta de la masa del hidrógeno a partir de su volumen y de la búsqueda de su densidad en unas tablas, en las condiciones de presión y temperatura en que se recoge.
¿Cómo recoger el gas hidrógeno y medir su volumen?
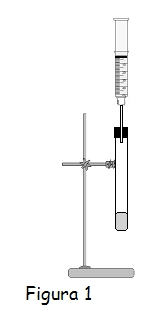
De nuevo existen varias posibilidades para resolver este subproblema. La respuesta de los estudiantes dependerá del conocimiento que puedan tener sobre los métodos de recogida de gases. Obviamente recoger el gas hidrógeno en un recipiente rígido no es aconsejable, por el aumento de la presión que se producirá. Una solución puede ser recogerlo en un recipiente con una pared móvil como, por ejemplo, una jeringa graduada (figura 1). En tal caso la presión del hidrógeno será igual a la presión atmosférica.
Otra posibilidad puede ser, aprovechando que el hidrógeno es insoluble en agua, recogerlo sobre sobre agua. Ésta es una técnica que es difícil que se les ocurra a los estudiantes si no la han utilizado previamente. La figura 2 muestra el dispositivo experimental que puede utilizarse.
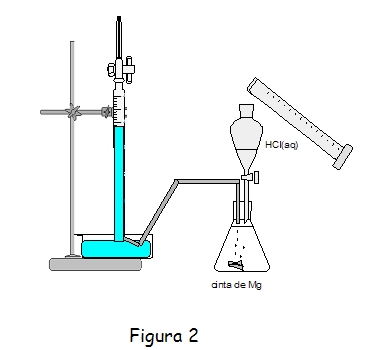
El hidrógeno es llevado a través de un tubo de goma a la parte inferior de un tubo lleno de agua invertido, cuya parte inferior ha sido sumergida en un vaso con agua. Si el tubo está graduado, podemos leer directamente el volumen de hidrógeno desprendido durante la reacción.
En este momento pueden surgir preguntas como las siguientes. ¿ Y si parte del hidrógeno se queda en el tubo de goma?, ¿Qué pasa si el hidrógeno ha arrastrado parte del aire al tubo graduado? En tal caso, ¿estaríamos midiendo exactamente el volumen de hidrógeno desprendido?. La respuesta es que sí; primero porque debido a la menor densidad del hidrógeno es éste el que burbujea y asciende a través del agua del tubo y, en segundo lugar, porque , aunque no fuera así, a presión constante el aumento de volumen de la fase gaseosa que se detecta sería igual al volumen del hidrógeno producido en la reacción, independientemente de que todo el hidrógeno se encuentre o no el tubo. A excepción del volumen parcial del vapor de agua que se haya podido vaporizar y se encuentre mezclado con el hidrógeno obtenido, que debería descontarse.
¿Cómo calcular la masa de hidrógeno a partir de su volumen?
Para calcular la masa de hidrógeno seco obtenido precisamos conocer la densidad y para ello precisamos conocer la temperatura y la presión del gas hidrógeno. La temperatura la podemos medir con un termómetro. La presión puede tomarse en primera instancia igual a la presión atmosférica. Una determinación más exacta requiere descontar la presión hidrostática debida a la columna de agua en el tubo. Y una determinación todavía más exacta, descontar la presión debida al vapor de agua. Otra opción es calcular la masa de hidrógeno a través de la ecuación de estado de un gas ideal. En realidad esta opción puede también utilizarse para calcular la densidad del hidrógeno y darla como dato a los estudiantes, en el caso que todavía no hayan estudiado la ecuación de los gases ideales.
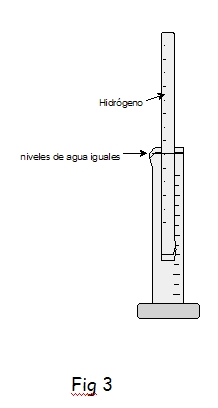
La corrección por la presión puede evitarse si extraemos el tubo con el hidrógeno, tapando su extremo inferior con el dedo o con un placa de vidrio, y lo trasladamos y sumergimos en una probeta suficientemente larga (fig 3). Desplazando el tubo graduado hacia abajo podemos hacer que coincidan los dos niveles de agua, el interior del tubo graduado y el exterior del probeta, con lo cual la presión del gas in terior es igual a la presión atmosférica.
¿Cómo se puede mejorar el dispositivo experimental?
Una cuestión que puede plantearse a los estudiantes es cómom podríamos intentar minimizar o evitar completamente la pérdida de hidrógeno que se produce al introducir el magnesio en el erlenmeyer. Podemos comenzar con la cuestión siguiente: ¿Qué es preferible, situar la solución de ácido clorhídrico en el erlenmeyer y verter el trozo de cinta de magnesio o al revés? Obviamente es más rápido echar un trocito de un sólido que verter una solución. Para verter ésta sin que hubiera pérdidas de hidrógeno, también podríamos colocar un embudo con llave ajustado en el tapón del erlenmeyer, pero entonces estaríamos desplazando un volumen de aire del interior del erlenmeyer igual al volumen que ocupa la solucion vertida, de tal manera que no todo el volumen de agua desplazada sería atribuible al hidrógeno formado.
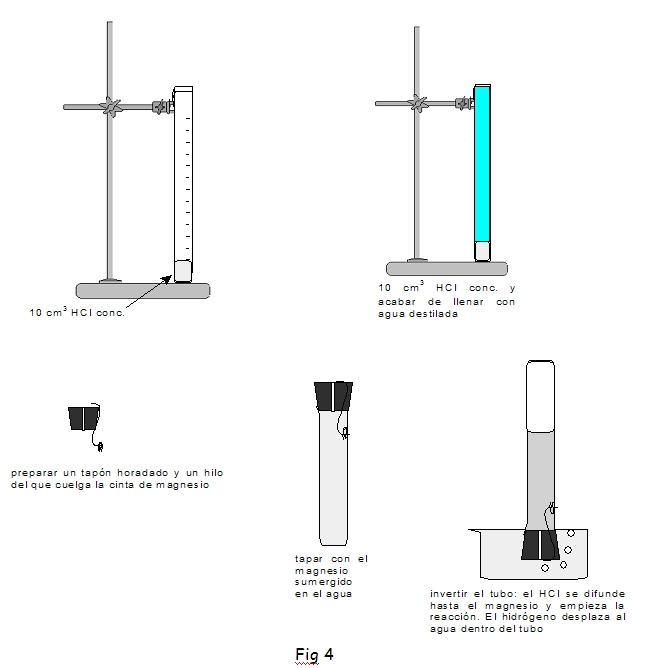
Otra posibilidad es hacer que la reacción tenga lugar directamente en el tubo graduado. Se coloca en el interior del tubo, antes de invertirlo, primero ácido clorhídrico concentrado y después agua destilada. Luego se suspende la cinta de magnesio con un hilo, que pasa entre el tubo y un tapón horadado, de manera que quede sumergida dentro del agua destilada. A continuación se tapa el tubo con el dedo y se invierte, introduciéndolo en un vaso con agua. El ácido clorhídrico difunde y cuando se pone en contacto con el magnesio tiene lugar la reacción. El hidrógeno que se produce desplaza un volumen equivalente de agua. Para poder efectuar la lectura del volumen a la presión atmosférica se procede como en el caso anterior: se traslada el tubo a una probeta y se sumerge hasta que coinciden los niveles. El procedimiento descrito se muestra en la figura 4.
Unos grupos de estudiantes pueden utilizar uno de los métodos sugeridos y otros el otro, con la finalidad de comparar posteriormente los resultados.
¿Qué cantidad de magnesio debemos utilizar?
Una cuestión práctica que se nos planteará en el momento de realizar la experiencia es decidir qué cantidad de magnesio debemos tomar para que no se produzca un volumen de hidrógeno superior a la capacidad del tubo de recogida. Otra cuestión es; ¿cómo podemos medir con el mínimo error esta cantidad de magnesio, que probablemente estará en el límite de la sensibilidad de la balanza de que disponemos? Por último debemos decidir cuál es la concentración más adecuada de la solución de ácido clorhídrico que debemos utilizar.
REALIZACIÓN DE LA EXPERIENCIA, TRATAMIENTO DE LOS DATOS Y COMUNICACIÓN
Cálculo de la masa atómica relativa del magnesio
Una vez obtenido el valor del volumen de hidrógeno, podemos calcular su masa y, a partir de este dato, la masa atómica relativa del magnesio de acuerdo con la relación establecida anteriormente.
Evaluación del resultado
Llegados a este punto es el momento de preguntarse: ¿es el resultado obtenido plausible? En nuestro ejemplo, podemos determinar el error relativo cometido contrastando el valor de la masa atómica relativa obtenido con el que viene tabulado en una tabla de masas atómicas relativas. Esto nos permitirá comparar la idoneidad de los dos métodos utilizados. Podemos también pedir un análisis de cuál debe ser la causa o causas principales del error cometido.
Comunicación de la investigación realizada
Finalmente llega el momento de convertir las notas tomados a lo largo de toda la investigación en un informe escrito y de preparar la presentación oral por parte de alguno de los grupos. Por lo que respecta a la producción escrita que les pedimos a los estudiantes a lo largo de la investigación (diario de la investigación) y en el informe final, es importante animarlos a utilizar con profusión dibujos, diagramas y ecuaciones para comunicar el fundamento teórico del método propuesto, y dibujos secuenciados, tipo viñeta, para mostrar cada una de las operaciones del método experimental propuesto. Especial atención deberá prestarse al uso adecuado de la terminología, a la escritura correcta de las magnitudes, tablas y gráficos, a la expresión adecuada de los cálculos y de las cifras significativas correctas, de acuerdo con la sensibilidad de los instrumentos utilizados
Comentarios finales
Las cuestiones estructuradas que hemos ido planteando permiten ir avanzando en la resolución del problema conjuntamente con los estudiantes. Unas han permitido comprender el problema a resolver y pensar un método de resolución, otras han permitido ir precisando el procedimiento, decidiendo qué variables debían ser medidas y cómo debían ser medidas; otras nos han permitido pensar sobre correcciones o dispositivos alternativos para mejorar la exactitud del resultado; por último, otras han permitido obtener y evaluar el resultado.
A lo largo de toda la investigación los estudiantes han estado “acompañados” por el profesor o profesora. En la fase de presentación y planificación del problema a resolver, que puede haber transcurrido perfectamente en el aula; en la fase de la realización de la experiencia, que necesariamente ha de tener lugar en el laboratorio; y en la fase de tratamiento de los datos, y de la obtención y evaluación del resultado, que puede muy bien volver a tener lugar en el aula. Sólo cuando se ha finalizado esta última fase, se pide a los estudiantes la escritura de un informe. En nuestra opinión tanto las fases de tratamiento de los datos, de evaluación del resultado e incluso, la de la escritura del informe deben realizarse en el aula en interacción con los estudiantes. Por último, la presentación oral de la investigación realizada es una actividad altamente recomendable para mejorar las habilidades comunicativas de los estudiantes.
¿Cómo convertir los trabajos prácticos tradicionales en trabajos investigativos?
Como decíamos al inicio, muchos trabajos de investigación muestran que la principal causa de ineficacia y de falta de motivación por el trabajo práctico viene dada por una presentación cerrada de estas actividades mediante guiones tipo “receta de cocina”. Las respuestas a las cuestiones planteadas en la investigación que acabamos de considerar son justamente las que vienen dadas en los protocolos cerrados de prácticas que se utilizan tradicionalmente. En el mejor de los casos estos guiones contienen un apartado final con cuestiones que intentan hacer reflexionar al estudiante a posteriori sobre el porqué de algunas de las instrucciones que le han sido dadas. De modo que, primero se les hace hacer todo sin darles oportunidad de pensar sobre nada y, después, se intenta paliar la propuesta “mecanicista” seguida con alguna pregunta reflexiva.
Si estamos dispuestos a enfocar los trabajos prácticos como investigaciones, la cuestión que se nos plantea es cómo deben ser los guiones escritos para que ayuden y orienten a los estudiantes en la planificación y realización de estas investigaciones. En un artículo reciente (Caamaño 2002) hemos abordado esta cuestión desde el punto de vista de cómo transformar los trabajos prácticos tradicionales en trabajos prácticos investigativos. El nuevo tipo de guión debe estructurarse a través de los apartados que corresponden a las fases de la investigación: 1. Planteamiento del problema; 2. Planificación (tanto del método experimental como de los cálculos necesarios para la obtención del resultado); 3. Realización experimental. 4. Tratamiento de los datos. 5. Evaluación del resultado; 6. Comunicación de la investigación realizada. En los dos primeros apartados pueden formularse por escrito la serie de cuestiones que hemos planteado a lo largo de la descripción dialogada de la investigación que nos ha servido como ejemplo y en el resto podemos recordar las tareas que deben realizarse (cuadro 1).
Cuadro 1. Ejemplo de esquema del guión abierto para una investigación
¿Cómo determinar la masa atómica relativa del magnesio?
Planteamiento del problema
• ¿Cómo determinar la masa atómica relativa del magnesio?
Justificación del interés de la investigación.
Planificación
• ¿Qué método indirecto de medida podemos utilizar?
• ¿Qué reacción podemos utilizar?
• ¿Qué medidas y cálculos es preciso realizar?
• ¿Cómo medir la masa del magnesio y la masa del hidrógeno?
• ¿Qué cantidad de magnesio es conveniente utilizar?
• ¿Cuál es la concentración más adecuada del ácido clorhídrico?
• ¿Cómo podemos recoger el gas hidrógeno y medir su volumen?
• ¿Cómo se puede calcular la masa de hidrógeno a partir de su volumen?
• ¿Cómo se puede mejorar el dispositivo experimental para evitar pérdidas de hidrógeno?
• Haz un esquema del procedimiento y del dispositivo que piensas utilizar y una lista del material y productos que precisas, atendiendo a los iconos de riesgo que vienen indicados en los contenedores de los productos.
Realización experimental
• Monta el dispositivo experimental, lleva a cabo la reacción y mide la masa del magnesio y el volumen del gas hidrógeno a presión atmosférica.
Tratamiento de los datos
• Realiza los cálculos para obtener el valor de la masa atómica relativa del magnesio.
Evaluación del resultado
• ¿Es el resultado plausible?
• Comprara el resultado obtenido con un valor tabulado
• Calcula el error relativo cometido. ¿Cuáles pueden ser las causas del error?
Comunicación de la investigación
• Escribe un informe que describa la investigación realizada y el resultado obtenido.
• Prepara una exposición oral de la investigación realizada con la ayuda de transparencias o el power-point.
Estos guiones abiertos, que pueden venir acompañados de hojas de ayuda y de unas orientaciones para el profesorado, constituyen una excelente manera de presentar por escrito una trabajo investigativo y guiar su resolución. Pero, en nuestra opinión, su mayor utilidad reside, especialmente en lo que se refiere a las fases de planteamiento y planificación, en sugerir las cuestiones que el profesor o profesora puede plantear a sus alumnos a la manera del diálogo propuesto en este artículo. Obviamente el guión también puede ser seguido por los propios estudiantes por sí solos. Es evidente que cabe una variedad de formas de utilización de estos guiones, según el tipo y complejidad de las investigaciones propuestas y el grado de conocimiento conceptual y procedimental de los estudiantes.
La principal objeción que se presenta a un planteamiento abierto como el que acabamos de proponer es que requiere más tiempo. Y esto es cierto. Pero, ¿acaso no es mejor hacer menos prácticas y que éstas sean más provechosas e ilustrativas de lo que es el trabajo científico? Otra dificultad fundamental para la incorporación de este enfoque abierto en los trabajos prácticos es que supone un cambio de mentalidad sobre el papel del profesor en la organización del trabajo de los estudiantes. Por lo que respecta a este último punto, creemos que tan sólo la oportunidad de vivir experiencias compartidas en seminarios y talleres con otros profesores, de reflexionar en equipo y de experimentar enfoques más abiertos podrá permitirnos avanzar en la transformación de los trabajos prácticos en una actividad más motivadora, creativa y eficaz para el aprendizaje de la comprensión conceptual y procedimental de la ciencia.
Referencias bibliográficas
• CAAMAÑO, A. (2002): ¿Cómo transformar los trabajos prácticos tradicionales en trabajos prácticos investigativos?, en Aula de innovación educativa, 113-114, pp.21-26.
• CAAMAÑO,A. (2003). Los trabajos prácticos en ciencias, en M.P. Jiménez(coord) et al. Enseñar Ciencias. Barcelona. Gráo.
• CAAMAÑO,A., COROMINAS,J. (ed.), (2002): Treballs pràctics de Química. Materials de formació. Batxillerat. Barcelona. Departament d’Ensenyament. Generalitat de Catalunya.
• CARRASCOSA,J. (1995): Trabajos prácticos de física y química como problemas, en Alambique, 5, pp. 67-76.
• GÁRRITZ, A. (2004): El trabajo práctico integrado con la resolución de problemas y el aprendizaje conceptual en la química de los polímeros, en Alambique, 39, pp.
• GIL, D., VALDÉS, P. (1996): La orientación de las prácticas de laboratorio como investigación: un ejemplo ilustrativo. Enseñanza de las Ciencias, 14, 2, pp. 155-163.
• GOTT, R., DUGAN, S. (1995): Investigative work in the science curriculum. Open University.
• HERNÁNDEZ, J. (2004). Análisi de una mezcla de carbonato y bicarbonato:una aproximación al trabajo científico. Alambique, 39, pp.
• MARTINS, I. (2002): Aprender a llevar a cabo una investigación en los primeros años de escolaridad, en Aula de innovación educativa, 113-114, pp. 14-17.
• OLDSWORTHY,R., WATSON,R. Et al (2001): AKSIS Project. Hatfield. ASE.
• QUALTER, A., STRANG,J., SWATTON,P., TAYLOR, R. (1990). Exploration. A way of learning science. Oxford. Blackwell Education.
• WATSON, R. (1994): Diseño y realización de investigaciones en las clases de ciencias. Alambique, 2, p.57.