Publicado en Alambique
Resumen
Las actividades llamadas POE (Predicción-Observación-Explicación) son una poderosa herramienta para la enseñanza de las ciencias al poner al alumnado frente a un fenómeno y obligarlo a que active sus ideas para hacer una predicción acerca de lo que espera que ocurra, para, después de observar el fenómeno, encontrar una explicación de lo que ha observado basada en un modelo. En este artículo se proponen varios ejemplos de física y de química de cómo trabajar en el aula este tipo de actividades
Introducción
Los profesores de secundaria nos encontramos con que muchos de los contenidos que se imparten a los estudiantes en las clases de ciencias tienen un nivel de abstracción elevado, que exige una manera de razonar muy formal. Para acabar de complicar la situación, no siempre es posible combinar las actividades que necesitan un laboratorio con la disponibilidad y equipamiento que tiene el centro.
Teniendo en cuenta que la interpretación de los fenómenos científicos por parte de los alumnos se basa en aquellos hechos y experimentos que ve, prueba, toca, huele o siente. Por otra parte, las analogías, metáforas o modelos juegan un papel importante en la construcción del conocimiento por parte de los estudiantes, resulta que los trabajos prácticos que obliguen a razonar son una herramienta esencial en esta tarea del aprendizaje. La indagación y la experimentación son competencias específicas de cualquier disciplina científica.
Se hace necesario por tanto, disponer de una diversidad de actividades que no se limiten a la descripción del experimento o al uso de una simulación o a la mera visualización de un video. Hay que activar los conocimientos previos de los estudiantes, y la argumentación y el análisis de lo que se ha presenciado. Son necesarias por tanto, actividades prácticas que ayuden a nuestros alumnos a relacionar hechos con modelos, y fenómenos observados con predicciones realizadas previamente (Corominas & Lozano,1994).
Por todo ello, las actividades prácticas conocidas como POE (Predicción-Observación-Explicación) son una herramienta altamente recomendable. Este instrumento (Chamizo,1997) implica tres pasos sucesivos: 1) Frente a un determinado evento se hace una predicción sobre aquello que se supone ocurrirá, justificando esta predicción; 2) Se describe qué es lo que sucede al llevarse a cabo el evento; 3) Se compara la predicción con la observación y se busca una nueva explicación si la que se ha dado no resulta satisfactoria.
En el primer paso se pretende poner en evidencia las ideas previas de los estudiantes respecto al evento o fenómeno propuesto. Tales ideas pueden ser consecuencia de conocimientos sobre el fenómeno que se va a realizar o simples “intuiciones” basadas a veces en suposiciones por asociación con hechos parecidos. El segundo paso requiere fijar la atención en lo que está ocurriendo y ser capaz de describirlo. A menudo se necesita tomar medidas y construir una tabla de datos. El tercer paso consiste en confrontar la predicción con lo que se ha observado.
Las actividades prácticas que se proponen a continuación están diseñadas siguiendo las orientaciones siguientes:
– Contextualizar la experiencia situándola en el marco de una secuencia didáctica (Caamaño et al., 2006), puesto que los actuales currículos de ciencias inciden especialmente en la contextualización de la ciencia (Caamaño, A. et. al., 2006).
– Animar a hacer una predicción del fenómeno, para analizar después si los hechos observados coinciden con la predicción. Esto permite en muchas ocasiones hacer aflorar las concepciones alternativas de los estudiantes.
– Potenciar la fase de la explicación del fenómeno. La explicación confrontada a la predicción permite al estudiante revisar sus ideas apoyándose en un modelo que le satisfaga.
Debe añadirse además la importancia de utilizar siempre que sea posible materiales y productos que se usan en casa o que son fáciles de encontrar en el comercio; la finalidad es poner en evidencia que la práctica científica no es exclusiva del laboratorio o del aula.
A continuación se describen siete ejemplos de actividades POE, que pueden realizarse sin dificultad en el aula normal de clase.
1. ¿Son aditivos siempre los volúmenes de líquidos?
Se preparan dos soluciones una de 100 mL de ácido clorhídrico de concentración 3 mol•dm-3 y otra de 100 mL de hidróxido de sodio de la misma concentración, 3 mol•dm-3. Ambas soluciones se presentan a los estudiantes en sendos matraces aforados y enrasados exactamente. Se pregunta: cuando se mezclen las dos soluciones en una probeta, ¿cuál será el volumen total y cómo se justifica la respuesta?
Hay que dar tiempo a que se elaboren diferentes hipótesis. Algunos estudiantes predicen un volumen total igual a la suma de los dos volúmenes, aduciendo la ley de conservación de la masa en las reacciones químicas. El profesor nunca deberá argumentar respecto a la predicción ni rectificar si la considera claramente errónea, más bien lo que hará será estimular a que se plantee alguna predicción más o que se admita esta cómo la única que el grupo ve posible. En otros casos, se predice que el volumen será mayor, sin especificar el nuevo valor, argumentando que la neutralización es una reacción exotérmica y se producirá una dilatación (en algunos casos predicen que la dilatación del la mezcla de líquidos se verá compensada por la dilatación del vidrio de la probeta, con lo cual el volumen total será de 200 mL). Algunos estudiantes recuerdan que el profesor unas semanas antes había mostrado cómo el volumen final de una mezcla de volúmenes iguales de agua y etanol es inferior a la suma de los volúmenes antes de mezclarlos; por lo tanto suponen que así ocurrirá también ahora, argumento que tiene muy poca solidez.
Cuando se hace el experimento, el volumen final es de unos 205 mL, fácilmente observables incluso con una probeta de sensibilidad 2 mL.
La explicación se hace evidente cuando se escribe la ecuación química de la reacción y se hace un cálculo de la cantidad de agua generada:
HCl(aq) + NaOH (aq) H2O(l) + NaCl(aq)
0,3 mol + 0,3 mol 0,3 mol + 0,3 mol
El volumen ocupado por la cantidad de agua formada en la neutralización es de 0,3 mol x 18 g/mol = 5,4 g; es decir 5,4 mL.
2. ¿Se moverá y hacia adonde?
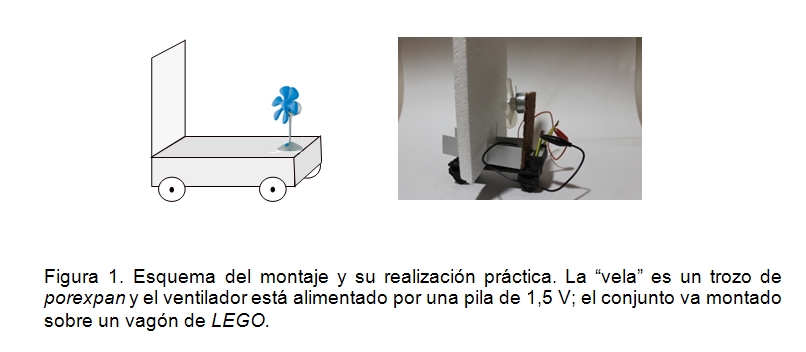
Se muestra a los estudiantes un pequeño carro que lleva montado un ventilador y una vela de gran superficie (figura 1) y se pregunta: ¿qué movimiento hará el carro cuando se ponga en marcha el ventilador?
Las posibles respuestas son:
– Se moverá hacia la izquierda
– No se moverá
– Se moverá hacia la derecha.
Después de debatir las diferentes predicciones siempre argumentadas, se pone en marcha el ventilador (que va accionado por pilas) y se observa que no hay movimiento alguno. En efecto se trata de un sistema en que solamente actúan fuerzas internas.
3. ¿Qué cubito fundirá antes?
Si se colocan tres cubitos de hielo colocados uno de ellos en una sartén, el otro sobre una madera y el tercero en un plato, ¿cuál fundirá antes?
Las predicciones deben tener en cuenta las capacidades caloríficas de los materiales, es decir con su conductividad térmica. Evidentemente, no hace falta esperar a que se funda completamente el trozo de hielo, basta con esperar unos minutos para ver que el que se ha colocado en la sartén funda primero.
Este experimento ha permitido que algunos estudiantes hayan recomendado en su casa que la mejor manera de descongelar un pescado o una carne es colocarla sobre una plancha metálica.
4. ¿Con o sin cáscara?
Una mandarina se pone en un recipiente con agua. La mandarina flota. ¿También flotará si le quitamos la cáscara?
La respuesta se deja para el lector. Como ayuda le proponemos que comprueba la flotabilidad de la cáscara de la mandarina o que examine atentamente su estructura altamente esponjosa.
5. ¿Cómo lo ves?
Se utiliza un puntero laser de color rojo que se proyecta en una pared y un papel transparente del mismo color rojo. Se pregunta: ¿Si dirigimos el rayo del laser de color rojo sobre el papel, continuaremos viendo el punto rojo en la pared?
Esta experiencia sirve para razonar sobre por qué vemos las cosas de determinados colores. Las respuestas permiten discutir sobre que colores se absorben cuando la luz atraviesa una vidriera de varios colores. Se puede completar la explicación, con una nueva pregunta: si el laser rojo se envía sobre una transparencia de color verde, ¿continuaremos viendo el punto rojo en la pared?
6. ¿Cuanto más mejor?
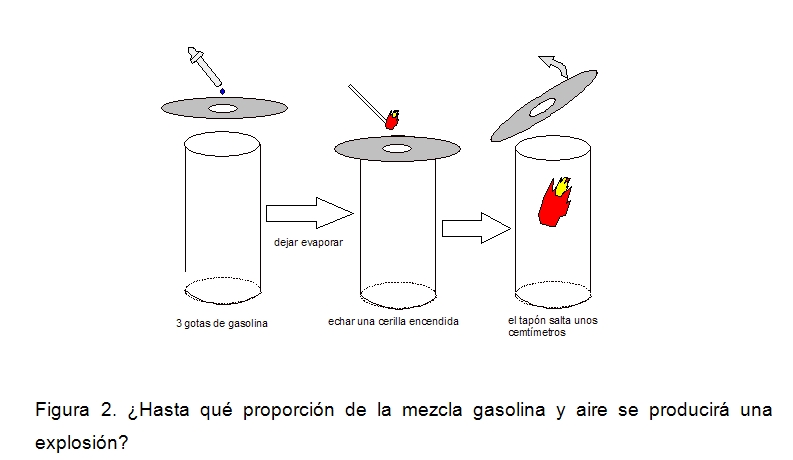
Se toma un recipiente cilíndrico de vidrio de un litro aproximadamente (no sirven los vasos de precipitados) por ejemplo un frasco de café soluble vacío. Sobre la boca del frasco se pone un círculo de cartón de diámetro algo mayor que el del frasco con un pequeño orificio central de 1 cm de diámetro. Con ayuda de un cuentagotas, se toma 1 mL de gasolina y se inyectan tres gotas a través del orificio. Se espera un minuto a que las gotas se evaporen. Se echa después una cerilla encendida a través del orificio, sin tocar los bordes. La mezcla explota inmediatamente, levantando el tapón unos centímetros. (Figura 2).
Se pregunta ahora ¿si aumentamos la cantidad de gasolina, habrá una explosión mayor? ¿Cada vez que aumentemos, irá a más la explosión?
Los estudiantes se sorprenden a menudo porque su predicción se basa en que a más gasolina, mayor explosión, olvidando que lo importante es mantener las proporciones estequiométricas entre los reactivos de la reacción, en este caso la gasolina y el oxígeno. Como sólo aumentamos uno de los reactivos, llega un momento que, incluso al echar la cerilla encendida dentro del frasco, esta se apaga, al haber sido desplazado el aire por la gasolina evaporada. A partir de este experimento se puede introducir el concepto de reactivo limitante.
7. ¿Cómo hinchar un globo con agua caliente?
Un líquido volátil es aquel que se evapora con facilidad, debido a su elevada presión de vapor por carecer de fuerzas intensas entre las moléculas. A mayor intensidad de las fuerzas intermoleculares, menor presión de vapor. Se trata de que los estudiantes relacionen la existencia de fuerzas debidas a enlaces de hidrógeno en las moléculas con la propiedad de volatilidad. Para ello necesitamos dos o tres líquidos de propiedades bien diferenciadas en cuanto a la facilidad de evaporarse. Por ejemplo, agua, etanol y acetona.
Presentamos tres globos de colores distintos, en los cuales hemos puesto en cada uno de ellos, uno de los tres líquidos antes citado. Es recomendable que sean volúmenes de entre 1 mL y 2 mL. Los globos se cierran anudándolos. Se prepara ahora un vaso de precipitados de 1000 mL con agua bien caliente. Se informa del contenido de cada uno de los globos y se pregunta ¿Cuál de los tres globos se hinchará más y más rápido, conociendo el tipo de moléculas que forman cada uno de los tres líquidos? ¿Cómo se justifica la respuesta en función de los enlaces posibles entre las moléculas?
El experimento es simple y permite que los estudiantes comprueben si sus predicciones eran las correctas: el globo que contiene la acetona, se hincha en unos segundos, al ser el líquido con mayor presión de vapor de los tres. El profesor, insistirá en la relación entre la estructura de la molécula y la debilidad de las fuerzas intermoleculares en la acetona.
Conclusión
Con estos ejemplos se ha pretendido dar una visión sobre las actividades POE. En realidad la mayoría de los experimentos del tipo demostraciones admiten plantearse como actividades del tipo predecir-observar-explicar.
Los experimentos del tipo demostraciones en el laboratorio o en el aula son útiles siempre y cuando no se limiten a la mera demostración y explicación “correcta” por parte del profesor. La condición indispensable para que sean provechosos está en hacer un uso consciente de las experiencias, teniendo en cuenta la manera como aprenden los estudiantes. Por ello, todo experimento debe ser debatido, analizado, criticado y sometida a contraste cualquier posible interpretación suministrada por los alumnos
Los experimentos de predicción-observación-explicación pueden ser un método idóneo para estimular el interés por la ciencia; sin olvidar que no son más que el primer eslabón que sirve para captar el interés y permitir después a cada estudiante ampliar el campo de la experimentación, diseñando nuevas experiencias que le permitan responder a nuevas cuestiones que se puede plantear.
Se recomienda que en algunos casos se utilicen actividades POE en que sea suficientemente fácil de predecir lo que sucederá para evitar la actitud de algunos estudiantes que razonan simplemente diciendo el contrario de aquello que suponen que sucederá, simplemente porque llegan a desconfiar de sí mismos.
Bibliografía
Chamizo, J. A. (1997). Evaluación de los aprendizajes. Tercera parte: POE, autoevaluación, evaluación en grupo y diagramas de Venn. Educación Química, 8, 141-143
Caamaño, A., Corominas, J., Doménech, M., Lope, S., Oro, J. y Plana, O. (2008). Los nuevos currículos de física, química y biología en el bachillerato de Cataluña. Alambique, 56, 51-70.
Caamaño, A. (coord.) (2011). Física y química. Investigación. Innovación y buenas prácticas. Barcelona: Graó.
Caamaño, A. (2004) Experiencias, experimentos ilustrativos,, ejercicios prácticos e investigaciones. Alambique, 39, 8-19.
Corominas, J. , Lozano, Mª T. (1994). Trabajos prácticos para la construcción de conceptos: experiencias y experimentos ilustrativos, Alambique, 2, 21-26.