Publicado en Alambique, 1999
El aparato descrito a continuación proporciona excelentes resultados para determinaciones cuantitativas.
Es especialmente útil para comparar calores de combustión de una serie de alcoholes: etanol, propanol, butanol, pentanol y también gas metano y gas butano.
Material para la construcción del Calorímetro:
– Lata de conservas vacía del tamaño de 3/4 de litro
– 1 m de tubo de cobre de 5 mm de diámetro interno
– Lana de vidrio o fibra de vidrio para aislante térmico
– Un adhesivo para metales que resista altas temperaturas ( por ejemplo NURAL 34)
– Alambre
– Herramientas: Alicates, taladro (opcional)
Todos los componentes se pueden encontrar en las ferreterías
Construcción:
Se empieza haciendo un agujero en el fondo de la lata de igual diámetro que el grosor del tubo de cobre.
Hay que doblar el tubo de cobre en forma de serpentín: cualquier recipiente cilíndrico sirve como apoyo para que se doble a su
alrededor de manera cómoda, el diámetro del serpentín debe ser unos dos centímetros menor que el de la lata.
Usar el adhesivo para soldar el serpentín en el agujero antes taladrado. El tubo no debe sobresalir por la parte inferior y sólo
asomar unos centímetros por la boca de la lata. figur. La unión del tubo de cobre con la lata debe quedar bien soldada y sin
fugas.
Colocar el aislante alrededor así como tela de fibra de vidrioa modo de una falda en trono a la base de la lata
¡PRECAUCION!: La fibra de vidrio puede provocar alergias. Debe evitarse inhalarla y mejor usar gauntes para manipularla
Un buen aislante térmico puede obtenerse de las cajas de “porexpan” con que se envasan las botellas de productos químicos. Se recorta la caja unos centímetros alrededor de uno de los huecos que sirven para colocar las botellas y que ajusta perfectamente al tamaño de la lata de conservas (puede incluso forrarse la lata con tela de fibra de vidrio para más seguridad antes de encajarla en el correspondiente hueco.)
El calorímetro está casi acabado. Falta únicamente buscar o recortar un disco de porexpan del tamaño de la boca de la lata y perforar tres orificios: uno para encajar el serpentín, otro para el termómetro y el tercero para un trozo de alambre que servirá de agitador.
Uso del calorímetro:
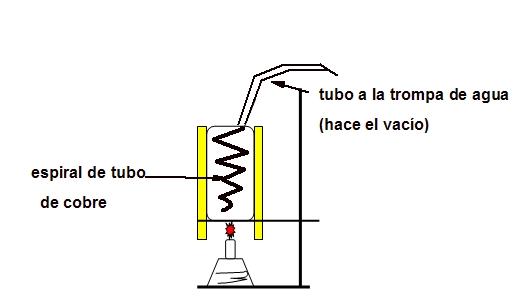
Tal como se indica en la introducción el calorímetro es especialmente útil para determinar entalpías de combustión de combustibles como alcoholes primarios y también gases. En cualquier caso debe realizarse el siguiente montaje. El calorímetro se llena de agua y se tapa.
La finalidad de la trompa de agua o bomba de vacío es mantener una corriente de aire que permita una combustión lo más completa posible.
Los gases producidos, al pasar a través del serpentín de cobre ceden su calor al agua, con lo cual se realiza una máxima transferencia de energía del combustible al agua, al aprovechar el calor producido por la llama y el de los gases. Conviene intercalar un matraz con agua entre la salida del serpentín y el aparato de vacío para controlar, por las burbujas, que hay suficiente aunque no excesivo “tiraje” por el serpentín.
Para combustibles líquidos usar lamparillas de alcohol, que deben pesarse antes y después de quemar durante unos minutos, para conocer la masa de combustible que ha quemado.
Si se pretende hacer un estudio comparativo del poder calorífico de una serie de alcoholes debe empezarse por determinar el “equivalente del calorímetro”. Para ello se quema una masa conocida de etanol, cuya entalpía de combustión es de 1371 kJ/mol. Supongamos que la masa quemada de etanol es m g, y el aumento de temperatura del agua del calorímetro de T ºC.
El número de moles consumidos de etanol es: m/46.
Su entalpía de combustión será H = m.1371/46 J
Y el equivalente del calorímetro C = H/ T
Ahora puede cambiarse la lamparilla de etanol por propanol, en esta caso bastará con efectuar las mediciones de incremento de temperatura T y número de moles consumidos n, puesto que la entalpía de
combustión se puede calcular a partir del equivalente del calorímetro:
H = C. T/n
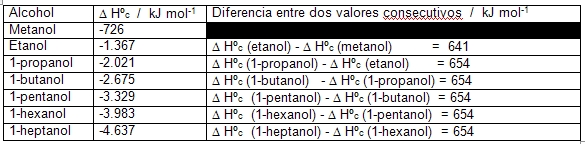
En la Tabla (1) están algunos resultados experimentales obtenidos, usando etanol para calcular el equivalente del calorímetro:
Obsérvese, además que si se calculan las diferencias de entalpía de combustión entre un alcohol y el siguiente en número de átomos de carbono, los valores son casi idénticos, siendo el valor promedio de 613 kJ/mol, este valor nos da una idea de la energía de enlace entre un grupo -CH2- y el resto de la molécula.