Publicado en Cuadernos de Pedagogóa
Adela Barral/Josep Corominas/Alejandro Gil/Mercè Izquierdo
Descripción de una experiencia de fácil realización. Se trata de ser capaces de cambiar el
color de los indicadores para clasificar las soluciones acuosas en ácidas, básicas y neutras.
CLASIFICANDO SOLUCIONES LÍQUIDAS MEDIANTE INDICADORES
Se trata de descubrir una interesante propiedad de las disoluciones acuosas de materiales de uso común y de sustancias corrientes en los laboratorios de química: la de ser capaces de cambiar el color de los «indicadores».
Con ello tendremos un criterio que nos permitirá clasificar las soluciones acuosas en ácidas, básicas y neutras.
Para ello el procedimiento consiste en preparar disoluciones acuosas de bicarbonato, aspirina, sal, caramelos, yogourt, jabón, lejía, salfumán, ceniza de cigarrillo, zumos de limón, manzana y tomate y azúcar. Se llenan con ellas pequeños recipientes (vasos, envases limpios de yogourt). Se utiliza también agua mineral con gas, agua de seltz y vinagre. Se corta luego a trocitos una tira de papel indicador universal y se moja en cada solución. Hay que observar el color que aparece en el papel y, según él, clasificar a las soluciones acuosas en ácidas (color desde naranja a rojo intenso), neutras (naranja verdoso) y básicas (verde claro a azul intenso).
A continuación, se utilizarán sustancias corrientes de laboratorio: amoníaco, hidróxido sódico, ácido clorhídrico,
carbonato de sodio, etc., para seguir ensayando con el papel indicador.
CAMBIO DE COLOR DE INDICADORES EN LA NEUTRALIZACIÓN
Esta experiencia consiste en añadir a una disolución diluida de ácido clorhídrico, una disolución diluida de hidróxido de sodio: veremos cómo cambia el color del papel indicador (mojando en la solución un nuevo papel después de cada adición). Con cuidado, añadiendo con un cuentagotas la solución adecuada, hay que conseguir una solución neutra: podemos beber esta «mezcla» de ácido y base, ya que sólo será agua salada. Si dejamos el
líquido sobrante en una cápsula hasta que se evapore el agua, obtendremos un poco de sal de cocina (cloruro de
sodio). Esta última experiencia permite comprobar que el ácido clorhídrico (salfumán) y el hidróxido de sodio
(sosa cáustica) forman cloruro de sodio.
¿CÓMO SE OBTIENENLOS INDICADORES?
Se prepara una solución de azul de bromotimol, disolviendo 0,1g de azul de bromotimol en 125 cc de etanol (Solución 1 ).
Se prepara también una solución de rojo de metilo disolviendo 0,1g de rojo de metilo en 250 cc de etanol (Solución 2).
Se debe comprobar que la solución 1 toma color rojo si se le añade la solución de salfumán o vinagre (ácidos), y que la solución 2 toma un color azul si se le añade una solución de amoníaco o lejía (bases).
Mojando un papel de filtro en las dos soluciones, obtendremos algo semejante al papel indicador que utilizamos en el apartado anterior.
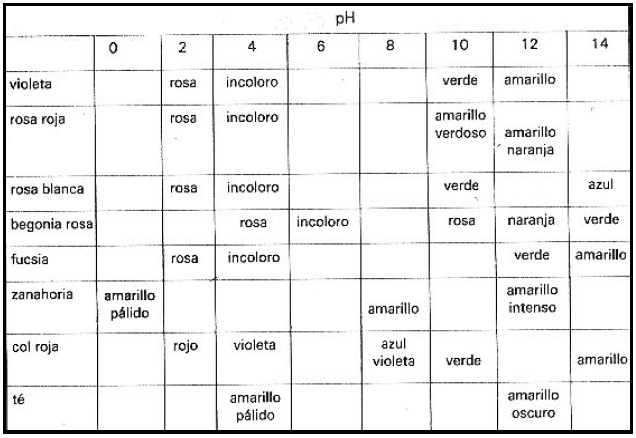
Las flores y otras plantas coloreadas contienen sustancias parecidas al rojo de metilo y azul de bromotimol y por eso pueden actuar también como indicadores de ácido-base. Presentan esta propiedad las violetas, rosas, geranios, buganvillas, malvas, begonias y otros vegetales comoté, zanahoria, remolacha, col lombarda, zumo de manzana y zumo de uva.
Se pueden obtener curiosos efectos al mojar estas flores con soluciones acuosas muy ácidas o muy básicas, por ejemplo salfumán o amoníaco (en general la acción del amoníaco es más eficaz si se mezcla con éter en la proporción de 9 partes -en volumen- de éter por una de amoníaco).
Para preparar un extracto (una solución indicadora) se pueden seguir los procedimientos siguientes:
· hervir la planta (previamente triturada) cubierta de agua. Filtrar y enfriar;
· machacar los pétalos de las flores en una mezcla de 2 mLde etanol y 2 mL de acetona. Filtrar;
· machacar los pétalos de las flores en etanol y calentar a ebullición la mezcla. Filtrar y enfriar.
Los colores que se obtienen varían con el «grado de acidez» o pH y son: